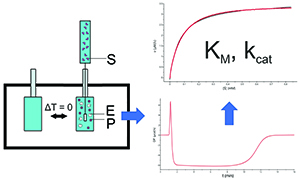
Mikrokalorymetria jako narzędzie w badaniach kinetyki enzymatycznej
DOI:
https://doi.org/10.18388/pb.2021_529Abstrakt
Enzymy jako katalizatory większości procesów w organizmach żywych stanowią istotny cel wielu terapii, mają też duże znaczenie przemysłowe, dlatego powtarzalna i dokładna parametryzacja katalizy enzymatycznej jest bardzo istotna nie tylko w badaniach podstawowych, ale też wdrożeniowych. Najbardziej popularna w enzymologii metoda detekcji spektrofotometrycznej, mimo niskich kosztów i szybkości, często nie może być zastosowana bezpośrednio z uwagi na nieodpowiednie właściwości spektralne substratów i produktów. Konieczne jest wtedy korzystanie z pomocniczych enzymów, modyfikacji chemicznej substratów, bądź analizy poreakcyjnej, np. przy użyciu spektrometrii mas, co może zwiększać koszty pomiaru, wydłużać jego czas, bądź wpływać na dokładność oznaczeń. Izotermiczna kalorymetria miareczkowa jest metodą rozpowszechnioną głównie w celu charakterystyki oddziaływań między-molekularnych, jednakże jej użycie w kinetyce enzymatycznej zdobywa coraz większe uznanie z uwagi na bezpośredni pomiar prędkości reakcji przy użyciu uniwersalnego parametru jakim jest ciepło, brak konieczności stosowania sztucznych substratów lub przetwarzania poreakcyjnego, a także wysoką czułość i niskie zużycie reagentów. Niniejsza praca omawia dwie strategie przeprowadzania kinetycznego eksperymentu kalorymetrycznego, a także ich przykładowe zastosowania.
Pobrania
Opublikowane
Licencja
Prawa autorskie (c) 2024 Joanna Śliwiak, Anna Urbanowicz

Utwór dostępny jest na licencji Creative Commons Uznanie autorstwa 4.0 Międzynarodowe.
Zawartość kwartalnika jest rozpowszechniana na licencji Creative Commons Uznanie autorstwa 4.0 Międzynarodowe (CC BY 4.0). Uznanie autorstwa — Utwór należy odpowiednio oznaczyć, podać link do licencji i wskazać jeśli zostały dokonane w nim zmiany . Możesz to zrobić w dowolny, rozsądny sposób, o ile nie sugeruje to udzielania przez licencjodawcę poparcia dla Ciebie lub sposobu, w jaki wykorzystujesz ten utwór.
Prawa autorskie do prac © pozostają przy autorach.
Prawa autorskie do czasopisma © posiada Polskie Towarzystwo Biochemiczne.